Analyse des données publiques
Les données sur les lignées du SRAS-CoV-2 et la date de prélèvement de l'échantillon à partir des séquences disponibles au Chili ont été obtenues auprès du site Consorcio Genomas CoV2 disponible sur https://auspice.cov2.cl/ncov/chile-global. Les données de vaccination ont été obtenues à partir des données publiques du ministère de la Science, de la Technologie, de la Connaissance et de l'Innovation disponibles sur https://github.com/MinCiencia/Datos-COVID19 (Produit 83).
Test d'infectiosité
Des virus pseudotypés portant différentes protéines de pointe du SRAS-CoV-2 ont été préparés comme nous l'avons décrit précédemment12. En bref, des pseudotypes du SRAS-CoV-1 basés sur le VIH-2 ont été produits dans des cellules HEK293T en transfectant le pNL4.3-ΔEnv-Luc avec le vecteur codant pCDNA-SARS-CoV-2 Spike correspondant dans un rapport molaire de 1 : 1. Plasmides codant pour un pic optimisé en codons dépourvu des 19 derniers acides aminés de l'extrémité C-terminale (SΔ19) connus pour éviter la rétention au niveau du réticulum endoplasmique12 ont été obtenus par synthèse génique ou mutagenèse dirigée personnalisée (GeneScript) et contenaient les mutations suivantes : lignée A (séquence de référence), lignée B (D614G), lignée B.1.1.7 (Δ69-70, Δ144, N501Y, A570D, D614G, P681H, T716I, S982A, D1118H), lignée P.1 (L18F, T20N, P26S, D138Y, R190S, K417T, E484K, N501Y, D614G, H655Y, T1027I) et lignée C.37 (G75V, T76I, Δ 246- 252, L452Q, F490S, D614G, T859N). Chaque préparation de pseudotype a été éliminée par centrifugation à 3,000 1 tr/min à température ambiante, quantifiée à l'aide du kit ELISA HIV-24 Gag p50 Quantikine (R&D Systems), aliquotée dans 80 % de sérum de veau fœtal (Sigma-Aldrich) et conservée à -1 °C jusqu'à utiliser. Différentes quantités de virus pseudotypés (déterminées par les niveaux de protéine p24 du VIH-2) ont été utilisées pour infecter les cellules HEK-ACE48 et 96 heures plus tard, l'activité de la luciférase de luciole a été mesurée à l'aide du réactif de test Luciferase (Promega) dans une microplaque Glomax XNUMX. luminomètre (Promega).
Essai de neutralisation
Les tests de neutralisation des virus pseudotypés ont été réalisés essentiellement comme nous l'avons décrit précédemment.12. En bref, des dilutions en série des échantillons de plasma (1: 4 à 1: 8748) ont été préparées dans du DMEM avec 10% de sérum de veau fœtal et incubées avec 5 ng de p24 de chaque virus pseudotypé pendant 1 heure à 37 ° C, puis 1 × 104 Des cellules HEK-ACE2 ont été ajoutées à chaque puits. Des cellules HEK293T (n'exprimant pas ACE2) incubées avec le virus pseudotypé (lignée A) ont été utilisées comme contrôle négatif. Les cellules ont été lysées 48 heures plus tard et l'activité de la luciférase de luciole a été mesurée à l'aide du réactif de dosage de la luciférase (Promega) dans un luminomètre pour microplaques Glomax 96 (Promega). Le pourcentage de neutralisation pour chaque dilution a été calculé et l'ID50 de chaque échantillon a été calculée à l'aide de GraphPad Prism version 9.0.1.
analyses statistiques
Les analyses statistiques ont été effectuées à l'aide du logiciel GraphPad Prism version 9.1.2. Des comparaisons de groupes multiples pour les titres d'anticorps neutralisants (NAbT) par rapport à un panel de virus pseudotypés du SRAS-CoV-2 ainsi que des comparaisons des réponses des NAb par sexe et statut tabagique ont été effectuées à l'aide d'un test signé-classé apparié de Wilcoxon. Le changement de facteur a été calculé comme la différence du titre moyen géométrique dans l'ID50 par rapport à celui du virus pseudotypé de type Wild. L'analyse de corrélation entre les NAbT et l'âge ou l'IMC a été réalisée à l'aide du test de Spearman. Une ANOVA unidirectionnelle et le test de comparaison multiple de Tukey ont été réalisés pour l'analyse statistique de l'infectiosité. Une valeur p ≤0.05 était considérée comme statistiquement significative.
Approbation éthique
Le protocole d'étude a été approuvé par le comité d'éthique de la Faculté de médecine de l'Université du Chili (projets N° 0361-2021 et N° 096-2020) et de la Clínica Santa Maria (projet N°132604-21). Tous les donneurs ont signé le consentement éclairé et leurs échantillons ont été anonymisés.
Impact des mutations de pointe dans la variante Lambda sur l'infectivité et les réponses en anticorps neutralisants
Une analyse de 3695 séquences du Chili déposées au GISAID au 24 juinth L’année 2021 montre une nette domination des variantes Gamma et Lambda du SRAS-CoV-2 au cours du dernier trimestre, représentant ensemble 79 % de toutes les séquences.
Il est intéressant de noter que cette période a été caractérisée par une campagne de vaccination massive au cours de laquelle 65.6 % de la population cible (individus de 18 ans et plus) ont reçu un schéma de vaccination complet au 27 juin.th 2021
Étant donné que 78.2 % des personnes vaccinées avec un schéma complet ont reçu le vaccin à virus inactivé CoronaVac de Sinovac Biotech, nous avons cherché à étudier l'impact des mutations de pointe présentes dans la variante Lambda sur la capacité neutralisante des anticorps produits par ce vaccin.
Pour cela, nous avons généré des virus pseudotypés SARS-CoV-1 basés sur le VIH-2 et portant la protéine Spike de la lignée de référence Wuhan-1 (type sauvage ; lignée A), de la mutation D614G (lignée B) et de l'Alpha (lignée B). .1.1.7), variantes Gamma (lignée P.1) et Lambda (lignée C.37).
Au cours de la préparation du virus, nous avons systématiquement observé que les cellules infectées par le virus pseudotypé portant le pic Lambda produisaient des valeurs de bioluminescence significativement plus élevées que celles du mutant D614G ou des variantes Alpha et Gamma, indiquant une infectivité accrue entraînée par la protéine de pointe Lambda.

Figure 1.Infectivité médiée par différentes protéines de pointe.
(A) Représentation schématique de la protéine de pointe du SRAS-CoV-2 et des variantes utilisées dans cette étude. Les lignées sont indiquées entre parenthèses. RBD, domaine de liaison au récepteur, CM ; queue cytoplasmique.
(B) Titrage des pseudotypes de chaque lignée en utilisant des quantités équivalentes de VIH-1 p24. L’activité luciférase de luciole a été mesurée en unités de luminescence relative (RLU) 48 heures après l’infection. La moyenne et l'écart-type ont été calculés à partir d'une expérience représentative en triple.
Ensuite, nous avons utilisé les virus pseudotypés mentionnés ci-dessus pour effectuer des tests de neutralisation en utilisant 79 échantillons de plasma provenant d'agents de santé en bonne santé de l'Université du Chili et de la Clínica Santa María à Santiago, au Chili.
Nous avons exclu 4 échantillons car nous n'avons pas pu calculer un titre ID50. Parmi les échantillons analysés, 73 % correspondaient à des femmes, d’âge médian 34 ans (IQR 29 – 43) et d’un indice corporel maximum (IMC) de 25 (IQR 22.7 – 27). 20.5% des participants ont déclaré être des fumeurs actifs pendant toute la durée de la période de vaccination. Les échantillons ont été obtenus dans un délai médian de 95 jours (IQR 76 – 96) après la deuxième dose du vaccin CoronaVac.
Nous avons observé que la neutralisation du virus pseudotypé portant la protéine Spike de type Wild entraînait une dilution inhibitrice de 50 % (ID50) titre moyen de 191.46 (154.9 – 227.95, IC à 95 %), alors qu'il était de 153.92 (115.68 – 192.16, IC à 95 %), 124.73 (86.2 – 163.2, IC à 95 %), 104.57 (75.02 – 134.11, IC à 95 %). ) et 78.75 (49.8 – 107.6, IC à 95 %) pour les virus pseudotypés portant respectivement la protéine Spike du mutant D614G ou des variantes Alpha, Gamma et Lambda.
Nous avons également observé que le titre moyen géométrique de l'ID50 les titres ont diminué d'un facteur de 3.05 (2.57 – 3.61, IC 95 %) pour le virus pseudotypé porteur du pic Lambda, 2.33 (1.95 – 2.80, IC 95 %) pour le pic Gamma, 2.03 (1.71 – 2.41, IC 95 %) pour le pic Alpha et 1.37 (1.20 – 1.55, IC 95 %) pour le pic D614G par rapport au pic de type Wild.
Aucune corrélation entre le sexe, l'âge, l'indice de masse corporelle (IMC) ou le statut tabagique et les titres d'anticorps neutralisants n'a été observée dans notre cohorte d'étude.
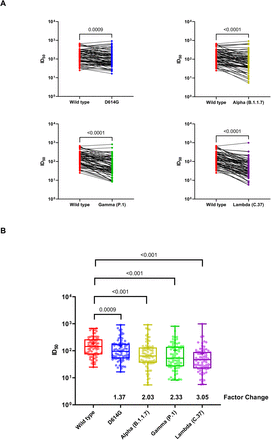
Figure 2.Test de neutralisation utilisant des échantillons de plasma provenant de vaccinés CoronaVac
(A) Modifications du titre de neutralisation réciproque à 50 % (ID50) dans des échantillons de plasma de 75 receveurs du vaccin CoronaVac contre le D614G (lignée B), Alpha (lignée B.1.1.7),
Variantes Gamma (lignée P.1) et Lambda (lignée C.37) par rapport au virus de type sauvage. Les résultats sont présentés comme la différence des titres de neutralisation des échantillons appariés. Valeurs P pour la comparaison de l'ID50 sont calculés avec le test de Wilcoxon signé-rank.
(B) Les boîtes à moustaches indiquaient la médiane et l'intervalle interquartile (IQR) de l'ID50 pour chaque virus pseudotypé. Les changements de facteurs sont représentés par la différence du titre moyen géométrique dans l'ID.50 par rapport à ceux du virus pseudotypé de type sauvage. Les analyses statistiques ont été effectuées à l'aide du test de rang signé par paires appariées de Wilcoxon.
Ensemble, nos données ont révélé que la protéine de pointe de la variante d'intérêt nouvellement reconnue Lambda, qui circule fortement au Chili et dans les pays d'Amérique du Sud, porte des mutations conférant une infectivité accrue et la capacité d'échapper aux anticorps neutralisants provoqués par CoronaVac.






















